

由中國臨床腫瘤學會(CSCO)主辦的"2020年中國臨床腫瘤學年度進展研討會"近日于線上順利召開,會上專家學者們對2020CSCO消化道腫瘤指南更新做了總結,近幾年頗受關注的免疫治療在新版指南中地位突顯,地位相較于舊版指南有所提升。
晚期食管癌二線免疫治療更新要點
卡瑞利珠單抗 I級推薦(鱗癌,1A類證據)
從本版指南的具體更新來看,對于"PS=0-2"的患者,I級專家推薦方案新增卡瑞利珠單抗(鱗癌,1A類證據)。
該推薦主要是基于隨機、開放、化療藥對照、多中心Ⅲ期臨床研究ESCORT研究結果,作為在中國晚期食管鱗癌患者中開展的首項、最大樣本的針對免疫檢查點抑制劑的研究,ESCORT研究共納入457例一線化療失敗的晚期或轉移性食管鱗癌患者(卡瑞利珠單抗組和化療組分別為228例和220例),分別接受卡瑞利珠單抗單藥治療(200 mg,每2周給藥一次)或研究者選擇的化療方案治療:多西他賽(75 mg/m2,每3周給藥一次)或伊立替康(180 mg/m2,每2周給藥一次)。結果顯示,與化療相比,卡瑞利珠單抗可顯著延長患者的中位生存期(mOS,8.3個月對6.2個月),降低死亡風險近30%,提高客觀緩解率(ORR,20.2%對6.4%),延長應答持續時間(DoR,7.4個月對3.4個月),并且無論PD-L1表達狀態,食管鱗癌患者相比化療都可以從卡瑞利珠單抗治療中獲益。在安全性方面,卡瑞利珠單抗的耐受性良好,安全、可控。卡瑞利珠單抗組≥3級藥物相關不良事件(TRAE)發生率僅為化療組的1/2(19.3%對39.5%)。
在研究方案上,ESCORT研究也充分考慮了中國食管鱗癌晚期一線治療多采用紫杉醇治療,二線化療對照藥物上選擇多西他賽或伊立替康,更適合中國的臨床實踐。綜合以上所述,新版指南發布會上專家們表示,ESCORT研究堪稱中國食管鱗癌免疫治療的里程碑研究。
帕博利珠單抗 I級推薦(鱗癌,PD-L1 CPS≥10,1A類證據)
帕博利珠單抗(鱗癌,PD-L1 CPS ≥10,1A類證據)由舊版指南中的III級專家推薦"晉升"為I級專家推薦,證據級別也由2B調整為1A。KEYNOTE-181研究中證實,相較標準化療,帕博利珠單抗可顯著改善既往接受過一次系統性治療的轉移性食管癌PD-L1陽性(CPS≥10)患者的OS。然而,KEYNOTE-181的研究中同時入組了鱗癌和腺癌患者,并且僅在CPS≥10的食管鱗癌患者中獲得了陽性結果。因此,FDA根據KEYNOTE-180及KEYNOTE-181審批的適應證也僅是針對接受過一線治療后病情進展,且PD-L1陽性(聯合陽性分數:CPS≥10)的復發性、局部晚期或轉移性食管鱗癌患者。在線上發布會上,專家們指出,帕博利珠單抗在后期補充的中國擴展隊列的研究中,入組的中國患者數量相對有限,僅在一定程度上體現了其在中國食管鱗癌患者中的療效。
納武利尤單抗 II級推薦(鱗癌,2A類證據)
納武利尤單抗由此前的III級專家推薦調整為II級專家推薦,證據級別由2B調整為2A。在ATTRACTION-3研究中,納武利尤單抗對419例晚期食管鱗癌患者的治療降低死亡風險23%,改善中位OS 2.5個月。新版指南發布會上,有專家表示,ATTRACTION-3入組的患者中并未包含中國患者,基于前文所述,中國與其他國家的食管癌患者存在諸多差異,因此,納武利尤單抗能否讓中國患者有同樣的獲益,還需要更多數據證實。
胃癌三線免疫治療更新要點
納武利尤單抗單藥,1A類證據,I級推薦(依據為ATTRACTION-2 III期研究);
ATTRACTION-2 III期研究結果:
納武利尤單抗組ORR為11.9%,中位應答時間1.6個月,療效持久,中位持續緩解時間長達9.8個月;
納武利尤單抗2y-OS率顯著高于安慰劑(10.6% vs. 3.2%,p<0.0001),治療緩解的胃癌患者生存更佳,中位OS長達26.6個月;
納武利尤單抗安全性和耐受性良好,治療相關不良反應發生率低且輕微,3/4級發生率僅10%。
帕博利珠單抗單藥適用于PD-L1 陽性聯合分數(CPS)≥1的患者,IB類證據,II級推薦(依據為KEYNOTE 059研究)。
KEYNOTE 059研究結果:
1.帕博利珠單抗用于晚期胃癌/胃食管結合部腺癌(G/GEJ)治療,ORR達11.6%,疾病控制率(DCR)27.0%,中位PFS 2.0個月,中位OS 5.6個月,12個月OS率為23.4%。
基于以上結果,2017年9月美國食品藥品監督管理局(FDA)批準帕博利珠單抗用于治療PD-L1表達陽性且既往治療后進展的晚期或轉移性胃癌或GEJ胃癌。
膽道腫瘤
一線治療更新要點:
I級專家推薦(1A 類證據):
(1)多納非尼
(2)貝伐單抗(A)聯合阿替利珠單抗(T)
1. 多納非尼:mOS達12.1個月
本次多納非尼的入選是基于ZGDH3 研究,該研究是多納非尼與索拉非尼的頭對頭比較,相對于索拉非尼,多納非尼更高效低毒,主要研究終點中位OS數據明顯優于索拉非尼(12.1 vs 10.3個月)。
2. "A+T"首次破冰十年來肝癌一線格局,成功延長OS及PFS
阿替利珠單抗是PD-L1單抗,貝伐珠單抗則是抗血管生成藥物。兩者聯合使用的"A+T"方案在2019年歐洲腫瘤內科學會亞洲大會(ESMO ASIA)上公布了IMbrave 150研究結果,成為10年前繼索拉非尼在HCC一線取得成功后的首次突破。
該III期研究納入了未經治的晚期HCC患者,隨機分為阿替利珠單抗+貝伐珠單抗組或索拉非尼組。主要研究終點包括OS及PFS。結果顯示,阿替利珠單抗和貝伐珠單抗組的中位OS較索拉非尼組顯著延長,為未達到vs 13.2個月(P=0.0006),降低了42%的死亡風險(HR 0.58)。
另一主要研究終點PFS方面,阿替利珠單抗和貝伐珠單抗聯合治療組為6.8個月,而索拉非尼組為4.3個月(P<0.0001,HR=0.59)。
III級專家推薦(2B類證據):
(1)侖伐替尼聯合帕博利珠單抗/納武利尤單抗
(2)化療聯合卡瑞利珠單抗
(3)阿帕替尼聯合卡瑞利珠單抗
二線治療更新要點:
I級專家推薦:
(1)卡瑞利珠單抗,2A類證據
(2)阿帕替尼,1A類證據
III級專家推薦(1A 類證據):
(1)納武利尤單抗聯合依匹單抗,2A類證據
1. 侖伐替尼聯合PD-1單抗療效初顯
侖伐替尼聯合帕博利珠單抗已獲FDA批準的突破性療法認定,該聯合方案的Ⅰb 期研究(KEYNOTE-524)在2020ASCO會議上更新了最新數據,中位OS達22.0個月(95% CI ,20.4~NE), 中位PFS達9.3個月(95% CI, 7.1~9.7),ORR達46% (95% CI ,36~56.3) ,CR達11%。
2020年ASCO-GI會議報告侖伐替尼聯合納武利尤單抗一線治療不可切除的HCC患者的Ⅰb期研究(Study-117研究),研究者依據 mRECIST 標準評估,總的ORR為76.7%,DCR為96.7%,臨床獲益率(CR+PR+SD 持續時間超過23周,CBR)為 83.3%。
2. 卡瑞利珠單抗聯合化療一線治療,初步數據令人滿意
一項卡瑞利珠單抗聯合FOLFOX4或GEMOX方案化療一線治療晚期HCC(肝細胞癌)或膽道腫瘤(BTC)患者全國多中心Ⅱ期研究中,在HCC隊列共有34例可評估的患者。結果顯示,經確認的ORR為26.5%,中位PFS為5.5個月,中位OS尚未達到,目前僅有3例(33.3%)患者出現了疾病進展。
3. 阿帕替尼聯合卡瑞利珠單抗,ORR高達50%
2018年10月發表于臨床腫瘤學雜志中的一項I b期研究結果顯示,卡瑞利珠單抗聯合甲磺酸阿帕替尼一線治療晚期肝細胞癌治療的客觀緩解率(ORR)高達50%,中位無疾病進展生存期(mPFS)達到7.2個月,6周的疾病控制率達到93.8%,療效顯著。
我們可以看到消化道腫瘤更新了眾多新方案,且這些新方案的研究結果大部分都是優于傳統治療方案。隨著近幾年全球新藥的火熱研發,腫瘤領域可說是迎來不少突破。除了免疫單藥治療之外,國產新藥及免疫+靶向聯合方案也取得了亮眼的成績。除此之外,全球仍有多項研究正在開展,包括免疫單藥、免疫+靶向、免疫+局部治療、免疫+免疫等,值得期待。希望這些研究能早日得出陽性結果,并獲批于臨床,讓更多患者能從中獲益。


全國共有49家實驗室報名參加,其中45家提交有效結果,僅23家通過評價活動,通過率為51.1%。

由中國臨床腫瘤學會(CSCO)主辦的"2020年中國臨床腫瘤學年度進展研討會"近日于線上順利召開,會上專家學者們對2020CSCO消化道腫瘤指南更新做了總結,近幾年頗受關注的免疫治療在新版指南中地位突顯,地位相較于舊版指南有所提升。
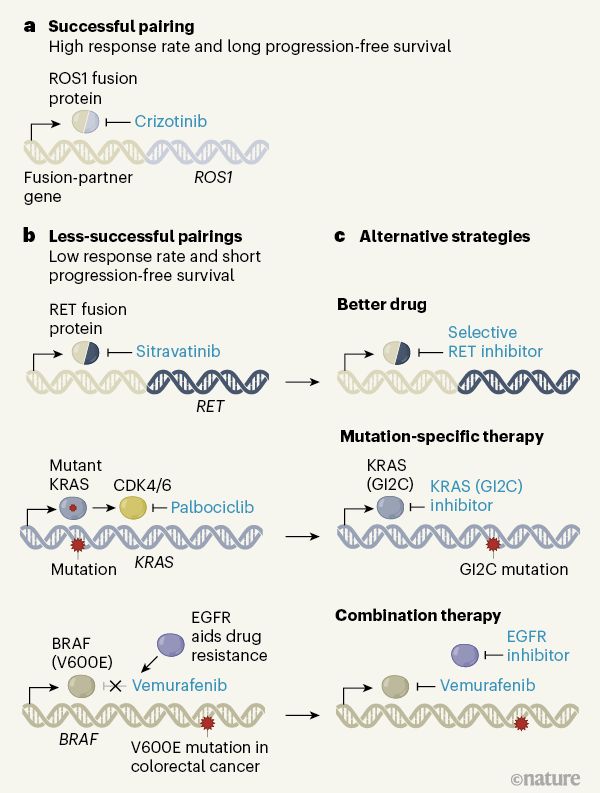
由伯明翰大學癌癥研究中心英國臨床試驗小組領導的一項開拓性的肺癌研究強調了下一波精準醫學研究,特別是治療基因組復雜癌癥需要考慮的重要因素。