

近年來,免疫檢查點抑制劑(immune checkpoint inhibitors, ICIs)為晚期驅動基因陰性NSCLC的治療帶來重大突破,患者5年生存率從化療時代的5%提升至13.4%~23.2%,ICIs已成為晚期NSCLC標準治療。但以EGFR基因突變為代表的驅動基因陽性NSCLC既往一直被認為是免疫治療的“禁區”,隨著對靶向藥物免疫調節作用的深入認識及臨床證據的不斷生成,免疫治療有望為驅動基因陽性NSCLC患者帶來新希望。由于驅動基因突變和靶向治療對于免疫微環境的影響較為復雜,臨床治療選擇也存在較多爭議,亟需規范化引導。在此背景下,中國抗癌協會腫瘤精準治療專業委員會和中華醫學會雜志社肺癌研究協作組共同組織多學科專家針對驅動基因陽性NSCLC免疫相關腫瘤及腫瘤微環境(tumor microenvironment, TME)特征和動態變化、ICIs臨床療效和安全性管理等多方面問題進行深入研討,形成專家共識,旨在更好地指導臨床實踐。
共識意見 1
不推薦ICIs用于晚期初治EGFR敏感突變NSCLC患者(推薦程度:一致不推薦)。
EGFR突變與腫瘤免疫原性低及非炎癥性微環境有關,且早期臨床研究表明,ICIs單藥或ICIs聯合化療治療初治EGFR敏感突變患者療效遠不及標準EGFR-TKIs靶向治療,然而,在EGFR-TKIs基礎上聯合ICIs的療效提升有限,且存在較大安全性風險。
共識意見 2
推薦耐藥的EGFR突變患者再次活檢,同時檢測腫瘤耐藥基因和免疫微環境相關的生物標志物(推薦程度:一致推薦)。
基于EGFR-TKIs治療會影響腫瘤特征和TME,建議條件允許的情況下應再次活檢,為后續精準治療提供依據。檢測標本優選腫瘤組織,組織標本無法獲得時可以采用其他類型標本替代;檢測范圍優選高通量檢測以獲得全面的耐藥信息,包括腫瘤相關和免疫微環境相關的生物標志物。
共識意見 3
對于EGFR-TKIs耐藥后發生廣泛進展的患者,且在缺乏有效靶向治療的情況下,推薦使用ICIs(推薦程度:一致推薦)。
對于ICIs的方案選擇,應結合患者的體能狀態和疾病進展情況進行綜合判斷,其中ICIs+化療+抗血管治療方案的臨床證據較為豐富(推薦程度:強推薦);ICIs+含鉑化療方案在多項早期研究中均顯示良好的治療活性,且耐受性方面ICIs+含鉑化療方案較ICIs+含鉑化療+抗血管聯合方案具有一定優勢(推薦程度:強推薦);ICIs聯合抗血管治療(推薦程度:弱推薦)的證據主要針對多線耐藥的患者或體力狀況較差不耐受高強度治療的患者,療效獲益有限。
共識意見 4
不推薦ICIs用于治療晚期初治ALK融合NSCLC(推薦程度:一致不推薦)。
ALK融合與腫瘤免疫原性低和非炎癥性微環境相關。多項早期研究結果一致提示ICIs聯合ALK-TKIs治療ALK融合NSCLC患者的療效提升有限,其中克唑替尼和塞瑞替尼聯合ICIs存在較大安全性風險。
共識意見 5
推薦ICIs聯合化療用于晚期初治KRAS突變NSCLC患者(推薦程度:強推薦)。
KRAS突變與腫瘤免疫原性高和炎癥性微環境相關。多項研究一致顯示,與單純化療比較,KRAS突變患者從ICIs中獲益更多,且一線治療中ICIs聯合化療的獲益多于ICIs單藥治療,此外KRAS G12C特異性抑制劑目前國內尚不可及,故針對KRAS突變NSCLC的患者推薦一線使用化療聯合ICIs。
共識意見 6
對于BRAF非V600E突變患者,推薦一線使用ICIs治療;對于BRAF V600E突變患者,推薦在靶向治療不可及或耐藥后發生廣泛進展時考慮使用ICIs治療(推薦程度:弱推薦)。
BRAF突變特別是非V600E突變與腫瘤免疫原性高和炎癥性微環境相關。多項回顧性研究一致顯示BRAF突變患者可從ICIs治療中獲益。
共識意見 7
伴有高危風險的患者使用免疫治療應謹慎,需要多學科評估與密切監測。EGFR-TKIs或ALK-TKIs與ICIs聯用存在很高的安全性風險,故不推薦同時使用。EGFR-TKIs和ICIs序貫使用需要關注洗脫期,以避免EGFR-TKIs與ICIs可能的疊加不良反應,洗脫期的設定需要考慮前序藥物的半衰期、器官功能恢復情況及疾病進展病情況,平衡治療安全性與療效獲益(推薦程度:一致推薦)。


全國共有49家實驗室報名參加,其中45家提交有效結果,僅23家通過評價活動,通過率為51.1%。

由中國臨床腫瘤學會(CSCO)主辦的"2020年中國臨床腫瘤學年度進展研討會"近日于線上順利召開,會上專家學者們對2020CSCO消化道腫瘤指南更新做了總結,近幾年頗受關注的免疫治療在新版指南中地位突顯,地位相較于舊版指南有所提升。
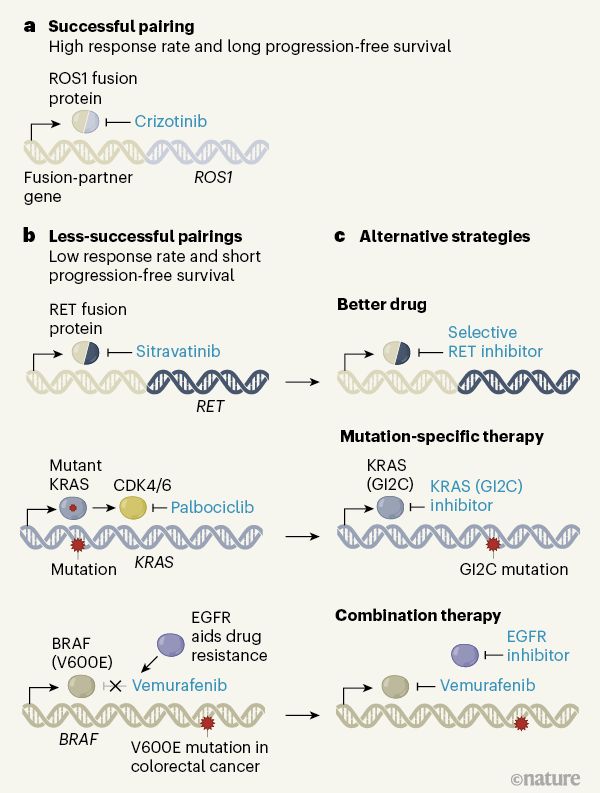
由伯明翰大學癌癥研究中心英國臨床試驗小組領導的一項開拓性的肺癌研究強調了下一波精準醫學研究,特別是治療基因組復雜癌癥需要考慮的重要因素。